工业高锰酸钾的制备 从二氧化锰到紫红色晶体
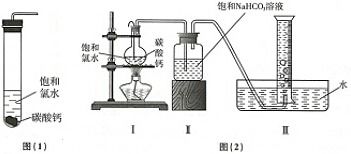
高锰酸钾(KMnO₄)作为一种重要的无机化合物,广泛应用于化工、水处理、医疗消毒及实验室分析等领域。其工业制备主要采用二氧化锰(MnO₂)和氢氧化钾(KOH)为原料,生产过程可分为两个核心步骤。
第一步:共熔氧化——制备锰酸钾(K₂MnO₄)
此步骤是制备过程的基础与关键。将原料二氧化锰(通常采用天然软锰矿粉)和固体氢氧化钾分别粉碎,以确保反应物之间能够充分、均匀地接触。将两者按一定比例(通常MnO₂稍过量)混合均匀。
混合物被置于特制的反应器(如铁锅或旋转炉)中,在空气中加热至其熔化(温度通常在250°C以上)。加热过程中,需要持续不断地搅拌。这一操作有多重目的:一是使物料受热均匀,防止局部过热;二是增加反应物与空气中氧气的接触面积,促进氧化反应的进行。
在高温熔融状态下,发生的主要化学反应为:
2MnO₂ + 4KOH + O₂ → 2K₂MnO₄ + 2H₂O
在此,空气中的氧气(O₂)作为氧化剂,将四价的锰(MnO₂中的Mn⁴⁺)氧化为六价的锰,生成绿色的锰酸钾(K₂MnO₄)熔体。因此,第一步的本质是在碱性介质中,通过氧化法制备锰酸钾中间体。
第二步:电解或氧化——将锰酸钾转化为高锰酸钾
得到绿色的锰酸钾熔体或溶液后,需要进一步将六价的锰(Mn⁶⁺)氧化为七价的高锰酸根(MnO₄⁻),从而制得目标产物高锰酸钾(KMnO₄)。工业上主要采用两种方法:
1. 电解氧化法(主流工艺):将第一步得到的含K₂MnO₄的碱性溶液进行电解。在阳极,锰酸根离子(MnO₄²⁻)失去电子被氧化为高锰酸根离子(MnO₄⁻):
MnO₄²⁻ → MnO₄⁻ + e⁻
阴极则产生氢气。此法产品纯度高,连续性好,是现代工业生产的主要方法。
2. 化学氧化法:向锰酸钾的碱性溶液中通入二氧化碳(CO₂)或加入稀酸(如醋酸),降低体系的pH值,使锰酸钾发生歧化反应,自身转化为高锰酸钾和二氧化锰:
3K₂MnO₄ + 2CO₂ → 2KMnO₄ + MnO₂↓ + 2K₂CO₃
生成的二氧化锰可以回收,返回第一步循环使用。此法简单,但产率相对较低。
通过第二步处理后,溶液变为特有的紫红色。再经过蒸发浓缩、冷却结晶、分离、干燥等一系列后处理工序,即可得到深紫色、有金属光泽的高锰酸钾晶体。
****,以MnO₂和KOH为原料制取KMnO₄的工业过程,巧妙利用了不同价态锰的转化。第一步在空气中共熔氧化,是制备关键中间体;第二步通过电解或化学方法完成最终氧化,体现了无机化工生产中对于反应条件控制和物质转化的精确把握。